هموکروماتوزیس یک اختلال سوخت و ساز آهن است
که ممکن است مادرزادی یا اکتسابی باشد. افراد مبتلا به هموکروماتوزیس
آهن بیشتری از نیازهای بدن خود ذخیره می کنند. بدلیل آنکه بدن راهی
برای دفع آهن اضافی ندارد، تجمع پیشرونده ای از آهن در بافت ها و اندام ها
وجود خواهد داشت.
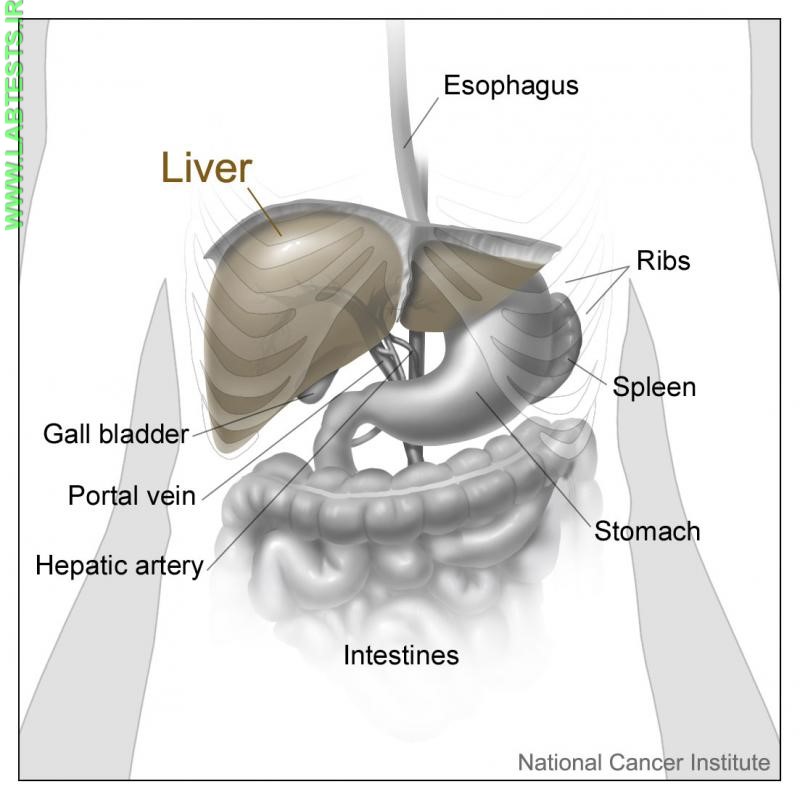
در نهایت مقادیر اضافی آهن می تواند موجب سوءکارکرد و نارسایی اندام های
مختلف بویژه قلب، کبد و بخش
درون ریز پانکراس شود. عوارض شامل آرتروز،
دیابت، سیروز کبد،
بی نظمی قلب و نارسایی قلب
و افزایش رنگدانه های پوستی به نام دانه های برنزه پوست می باشد.
دو نوع هموکروماتوزیس وجود دارد: هموکروماتوزیس اولیه (شکل ارثی که از یک
نسل به نسل بعد منتقل می شود) و هموکروماتوزیس ثانویه (که ناشی از بیماری
ها یا وضعیت های دیگر است).
هموکروماتوزیس اولیه یا ارثی (HH)
هموکروماتوزیس ارثی (HH) که هموکروماتوزیس اولیه نیز نامیده می شود، یکی از
شایع ترین اختلالات ژنتیکی در آمریکا است که بر حدود یک میلیون نفر (بیشتر
افراد قفقاز) اثرگذار بوده است. این بیماری اغلب ناشی از یک
جهش در ژن
HFE است. هر شخص دارای دو نسخه ژن HFE است که یک نسخه از مادر و یک
نسخه از پدر انتقال یافته است.
این جهش ها موجب تغییراتی در تجمع پروتئین ها (آمینواسیدها) می شوند و این
جهش ها توسط تغییراتی که در آمینواسیدها ایجاد می کنند، شناخته می شوند.
برای مثال، شایع ترین جهش شامل تغییر از یک آمینواسید به نام سیستئین (C)
به تیروزین (Y) در دویست و هشتاد و دومین آمینو اسید پروتئین ساخته شده
توسط ژن HFE است، این جهش با عنوان C282Y خوانده می شود.
جهش های مختلفی در ژن HFE وجود دارد که می تواند موجب هموکروماتوزیس
شود. احتمال افزایش مقادیر آهن وابسته به ترکیب ژن های ارثی است.
برای اطلاعات بیشتر در مورد ژن HFE به بخش زیر مراجعه کنید.
هموکروماتوزیس ثانویه یا اکتسابی
هموکروماتوزیس ثانویه، مقادیر آهن اکتسابی است که می تواند بدلیل برخی از
بیماری ها و وضعیت های دیگر باشد. مثالها شامل موارد زیر است:
-بیماری کبد مزمن مثل عفونت
مزمن هپاتیت C، بیماری کبد الکلی یا استیتوهپاتیت غیرالکی (NASH)
-سوءمصرف الکل
-برخی از شکل های کم خونی
-انتقال خون متعدد
-در موارد نادر، مکمل آهن خوراکی
Hemochromatosis
-
نشانه ها و علائم
طبق گزارش موسسه ملی قلب، ریه و خون، هر شخص مبتلا به هموکروماتوزیس دارای نشانه ها و علائم نخواهد بود و برآوردها در این مورد متفاوت است و در حدود نیمی از افراد مبتلا به بیماری ممکن است دارای علائم اولیه نباشند. نشانه ها و علائم از نظر شدت در طی زمان طولانی افزایش می یابد و می تواند مشابه با وضعیت های دیگر باشد.
معمولا، مردان تا سن 30 تا 50 سالگی دارای علائم این وضعیت نخواهند بود. بیشتر زنان مبتلا به هموکروماتوزیس تا چند سال بعد از توقف قاعدگی بدلیل یائسگی (تقریبا 50 سالگی) علائمی را تجریه نمی کنند.
نشانه ها و علائم از فردی به فرد دیگر متفاوت بوده و می تواند شامل موارد زیر باشد:
-خستگی، ضعف
-درد شکمی
-درد مفصل
-افزایش سطوح قند خون و دیابت
-نارسایی کبد و یا آزمایشات غیرعادی خون کبد
-کاهش میل جنسی، عدم توانایی جنسی در مردان
-فقدان قاعدگی در زنان
-کم کاری تیروئید
-تغییرات در رنگ پوست به طوسی یا برنز -
آزمایشات
آزمایشات زیر برای شناسایی و تشخیص هوکروماتوزیس و ارزیابی اندام های بدن برای ش دت بار اضافی آهن استفاده می شوند. این آزمایشات را همچنین می توان برای نظارت بر اثرگذاری درمان استفاده می شود. آزمایش ژنتیکی را می توان برای تایید یک تشخیص استفاده کرد، اما بدلیل آنکه بیشتر افرادی که دارای جهش های ژنتیکی مرتبط با بیماری هستند، هرگز علائمی را توسعه نمی دهند، آزمایشات خون بعنوان معتبرترین شکل تشخیص لحاظ شده اند.
بررسی های آزمایشگاهی
بررسی آزمایشگاهی معمولا شامل موارد زیر است:
-آهن خون- برای بررسی سطوح آهن در خون
-ظرفیت کلی اتصال آهن (TIBC)- برآورد مقادیر کلی آهن که می تواند متصل به پروتئین در خون باشد؛ ترانسفرین یک پروتئین اولیه متصل به آهن است و آزمایش TIBC برآورد غیرمستقیم خوب از قابلیت دسترسی به ترانسفرین است.
-اشباع ترانسفرین- برآوردی که از نتایج آزمایشات آهن و TIBC استفاده می کند و درصد ترانسفرین اشباع شده با آهن را بیان می کند؛ مقدار آن در هموکروماتوزیس ارثی (HH) افزایش می یابد اما مختص آن نیست.
-فریتین خون- برای ارزیابی ذخیره های آهن بدن؛ با HH افزایش می یابد اما مختص آن نیست. در افراد دارای ژن های HH، سطوح نرمال به معنی ریسک پایین برای آسیب به اندام است.
-پنل کبد- گروهی از آزمایشات مورد استفاده برای ارزیابی عملکرد کبد
-آزمایش ژنتیک- را می توان برای کمک به تایید تشخیص HH استفاده کرد. بیشتر موارد HH یعنی در حدود 80 تا 90 درصد ناشی از دو نسخه از یک جهش C282Y در ژن HFE است. وجود جهش C282Y ضرورتا به معنی این نیست که فرد آن اختلال را خواهد داشت بلکه نشانگر ریسک بالا است و مردان دارای احتمال ابتلای بیشتری از زنان هستند. بزرگترین تحقیق جمعیتی به ریسک 25 درصد در بین مردان و ریسک 1 درصدی در بین زنان دست یافت. گاها جهش H63D یا S65C از ژن HFE یا ترکیب هر سه می تواند موجب HH شود. در موارد نادر، این وضعیت می تواند بدلیل ناهنجاری ژنتیکی دیگری باشد.
-نمونه برداری از کبد- در موارد نادر، تشخیص با بررسی نمونه برداری های کبد از نظر تجمع آهن و آسیب به کبد، تایید می شود.
بررسی های غیرآزمایشگاهی
یک آزمایش MRI (تصویربرداری رزونانس مغناطیسی) را می توان برای کمک به ارزیابی مقدار آهن در کبد استفاده کرد. -
درمان
اهداف درمان هموکروماتوزیس، کاهش مقدار آهن در بدن و حفظ آن در غلظت های نزدیک به سطح نرمال، کاهش آسیب های دائمی به اندام و بررسی عوارض آن است. اگر شخصی دارای هموکروماتوزیس ثانویه باشد، در این صورت درمان باید به اختلال یا بیماری اصلی بپردازد. بدلیل اینکه همه افرادی که دارای تغییرات ژنتیکی هستند، نیاز به درمان ندارند، لذا فقط آن دسته از افرادی که در اثر آهن اضافی دارای آسیب اندامی هستند، تحت درمان قرار می گیرند.
هموکروماتوزیس اغلب با روش درمانی فلبوتومی، درمان می شود که معمولا شامل خارج کردن یک واحد خون است. تکرار و طول درمان وابسته به علت و میزان مقادیر اضافی آهن است، برای مثال، در افرادی که دارای مقادیر خیلی زیاد آهن هستند، فلبوتومی را می توان در ابتدا هفته ای یک بار یا دو بار انجام داد، اما بعد از حذف مقادیر اضافی آهن، فلبوتومی را می توان فقط چند بار در سال انجام داد.
هیچ روش درمانی برای هموکروماتوزیس ارثی وجود ندارد، اما می توان آن را بصورت موفقیت آمیزی در طی حیات یک فرد مدیریت کرد.
فردی که مبتلا به هموکروماتوزیس ثانویه است، در صورت رفع شدن علت اصلی بیماری، ممکن است به درمان طولانی مدت خون نیاز نداشته باشد، و اگر مقادیر اضافی آهن بدلیل انتقال خون مکرر باشد، در صورتیکه نیاز به انتقال خون پابرجا باشد، امکان انجام فلبوتومی وجود ندارد. داروهایی نیز وجود دارد که به آهن متصل شده و موجب ترشح آن به ادرار می شوند و این مورد را می توان برای افرادی استفاده کرد که نمی توانند به طور ایمن فلبوتومی را انجام دهند.
سازمان غذا و داروی آمریکا استفاده خون از بیماران هموکروماتوزیس را بعنوان دهنده خون تایید کرده است. برای اطلاع از مراکزی که بیماران مبتلا به هموکروماتوزیس می توانند برای اهدای خون خود مراجعه کنند، به صفحه انجمن هموکروماتوزیس آمریکا در این مورد مراجعه نمایید. -
ژن HFE
لیست زیر ترکیبات احتمالی ژن برای ژن HFE را بیان کرده است:
-دو نسخه از C282Y یا یک نسخه از C282Y به همراه یک نسخه از ژن های جهش پذیر H63D یا S55C موجب می شود فرد در بالاترین ریسک برای HH باشد.
-دو نسخه H63D، S55C یا یک نسخه از هر کدام از H63D یا S55C موجب می شود فرد در ریسک پایین باشد و در موارد خیلی نادر مرتبط با HH است.
-یک نسخه از C282Y، H63D یا S65C بدین معنی است که فرد حامل است. افراد حامل موجب توسعه بیماری نمی شوند، اما اگر زوج یا زوجه ای داشته باشند که او نیز حامل باشد، دارای فرزندان حامل خواهند بود.
البته، ژن های دیگر علاوه بر ژن HFE می توانند بر توانایی فرد در سوخت و ساز آهن تاثیرگذار باشند، بنابراین هیچ ترکیبی از ژن ها تضمین نخواهد کرد که فرد بیماری را توسعه دهد. برای مثال، چنین برآورد شده است که تنها در حدود 25 درصد از مردان و در حدود 1 درصد از زنان که دارای دو نسخه از جهش C282Y هستند، آسیب های اندامی مرتبط با آهن اضافی را توسعه خواهند داد.
HH بر مردان بیشتر از زنان موثر است و علائم بیماری در سنین پایین برای مردان (معمولا در 30 تا 50 سال) بروز می کند. دو شکل نادر دیگر از هموکروماتوزیس ارثی (نوزادی و جوانی) می توانند موجب افزایش شدید آهن در کودکان و بزرگسالان شوند. این بیماری ناشی از جهش در یک ژن متفاوت به نام hemojuvelin است. در واقع، درصد کمی از موارد HH بدلیل جهش در ژن های کد گذار برای پروتئین های دیگر شامل hemojuvelin و نیز گیرنده ترانسفرین 2، فروپورتین و هپسیدین هستند. با این حال، آزمایشات این جهش ها بطور گسترده موجود نیستند.
آزمایشها: TIBC, UIBC, and Transferrin, Ferritin, Serum Iron, Iron Tests, Liver Panel
بیماریها: Liver Disease (بیماری کبد), Inherited Hepatitis (هپاتیت مادرزادی)
ویژگیها: The Universe of Genetic Testing
American Hemochromatosis Society
American Hemochromatosis Society: Information on blood banks
Iron Disorders Institute
Centers for Disease Control and Prevention: Hemochromatosis (Iron Storage Disease)
National Digestive Diseases Information Clearinghouse: Hemochromatosis
National Heart, Lung, and Blood Institute: What is hemochromatosis?